Итак, настало время продолжения статьи о том, как все же сделать светящуюся елку к следующему новому году с применением настоящей генной инженерии, а не той, о которой вы до этого могли прочитать в новостях :)
Краткое содержание предыдущей серии:
Ученые открыли ген синего свечения. Мы прочитали об этом гене и загорелись сделать светящуюся трансгенную елку. Нашли в специализированных ресурсах его название и последовательность, выбили командировку у шефа и скатались туда, где живет животное – бутявка, в которой содержится этот ген.
Путем различных ухищрений с применением специального оборудования мы получили чистые молекулы ДНК гена bl1, кодирующего белок синего свечения.
У нас есть ген. Чего же мы ждем, спросят читатели, давайте засунем этот ген в елку и она начнет светиться?
Не все так просто, и вот, почему.
Любой ген работает только когда с него считывается информация. В нашем случае это мРНК белка bl1. Более того, сама мРНК должна работать, но это отдельная история.
Второе – ген должен передаваться при делении клетки ее потомкам. Иначе все пойдет насмарку.
Третье – ведь ген это не булавка, его еще засунуть как-то нужно!
Если мы просто поместим в клетку ген, то ни информация с него не будет прочитана, ни передаваться он не будет (да, собственно, и с засовыванием его большие проблемы). Поэтому, мы должны навесить на него какую-нибудь служебную информацию, которая бы позволила ему работать и облечь в форму, которая позволит передаваться потомкам. А так же каким-то образом занести его в клетку.
Однако еще раньше мы постараемся сохранить имеющийся ген, чтобы в любой момент можно было его получить много и не ездить за бутявкой.
Первая трансформация.
Самая первая задача, которая стоит на каждом этапе – сохранить результаты предыдущих этапов. Актуальная задачи и в программировании, не правда ли? :)
Сейчас мы поместим наш ген в бактерию, так, чтобы в любой момент мы могли ее размножить и достать оттуда необходимое количество. Это будет наш первый трансгенный организм и процесс его создания называется трансформацией.
Почему мы просто не можем размножить ген с помощью ПЦР, как мы делали до этого? Дело в том, что вероятность ошибки в реакции ПЦР 1/10^3, а в бактерии 1/10^6, то есть копирование его происходит в тысячу раз точнее, а точность нам нужна абсолютная и чем больше, тем лучше.
Итак, помещаем ген в бактерию, как же это сделать? Для этого для начала подготовим контейнер — специальную кольцевую молекулу ДНК, называемую плазмидой. Эта плазмида может плавать в клетке бактерии независимо от ее генома, размножаться и передаваться потомкам, так как у нее есть необходимые для этого гены и сигнальные последовательности.
Так же в плазмиде есть гены маркёры. Это такие гены, которые помогут нам отобрать клетки с плазмидой, от клеток где ее нет. Маркёром, например, может быть ген окраски (бактерии с плазмидой будут окрашены) или устойчивости (бактерии с плазмидой не умрут на среде с антибиотиком).
Плазмиды можно купить в биотехнологической компании, их продают всем желающим. Прийдет она к вам в виде прозрачного раствора в небольшой пробирке (собственно, так же выглядит раствор любой другой ДНК). Для вставки гена в плазмиду ее нужно надрезать ферментом — рестриктазой (речь о ней пойдет далее), но часто они продаются уже надрезанными.
Допустим мы купили современную плазмиду, например pJET1,2 от Fermentas.

Вот она, красавица. В верхнем правом углу много мелких названий – это перечислены сайты рестрикции. Rep – это участок отвечающий за репликацию (размножение) плазмиды в клетке, а Amp – репортерный ген устойчивости к антибиотику – ампициллину.
К плазмиде поставляется набор реактивов, так называемый “кит”. Мы капаем по инструкции чуть чуть раствора нашего гена, плазмиды с реактивами из кита и фермента лигазы и получаем раствор, где молекулы плазмиды соединились с молекулами гена и получилась единая кольцевая молекула, содержащая ген bl1.
Такую плазмиду называют “плазмида со вставкой”.
Фермент лигаза сшивает пристыкованые друг к другу участки ДНК. Она сшивает все подряд и не может определить, правильно ли все пристыковано (например, может просто сшить плазмиду саму с собой, вовсе без нашего гена), поэтому наша задача делать так, чтобы стыковаться молекулы могли только определенным образом. Чуть дальше я расскажу об этом, когда пойдет речь о липких концах.
Плазмида pJet1,2 продается уже разрезанной посередине гена eco471R. Это ген кодирует клеточный яд – мощную рестриктазу, которая убъет клетку если лигаза сошьет плазмиду без вставленного гена bl1 и такая плазмида попадет в бактерию. Это очень удобно, так как нам не нужно беспокоиться, что вырастут бактерии, в которых вовсе нет вставки, что бывает с другими типами плазмид (этот тип назван плазмидой-самоубийцей или “selfkill plasmid”).
Изначально эта информация выходила за рамки статьи, но я подумал, что иначе будут вопросы, зачем этот ген :)
Далее берем специально подготовленную культуру бактерий кишечной палочки (Echerichia coli или E.coli) и по протоколу трансформации капаем в них раствор плазмиды со вставкой. Протоколы могут быть разные, вот пример. Бактерии очень легко поддаются трансформации, по сути ДНК просто в них проникает и все, никаких других ухищрений.
Обычно трансформацию делают вечером, наутро бактерии подрастают и мы уже имеем результаты.
На чашке Петри со средой для роста, имеется множество колоний. Каждая колония — потомки одной единственной трансформированной клетки. Мы выбираем некоторые из них, тестируем на содержание bl1 методом ПЦР (чтобы убедиться в наличии гена) и можем положить на хранение.

Бактерии растут очень быстро и теперь плазмиду с геном можно выделить из них в любой момент в нужном количестве
Итак, мы засейвились :) и параллельно получили культуру трансгенных бактерий. Будут они светиться или нет зависит от того, какую плазмиду для трансформации мы выбрали, есть ли в ней сигнальная последовательность для синтеза мРНК – промотор.
Отмечу, что вот такое сохранение промежуточных результатов всегда проводят в бактериях, независимо от того, с каким далее объектом происходит работа. Просто с ними очень удобно работать и хранить (быстро заморозив в жидком азоте).
Подготовка транскрибирующейся последовательности.
Чтобы последовательность гена работала в клетке, с нее должна прочитываться мРНК(а с нее — белок), то есть она должна транскрибироваться. Для того чтобы это произошло, перед геном обязательно должна стоять управляющая последовательность – промотор.
Промоторы есть у всех генов и они отвечают за то, в каких условиях должен синтезироваться ген, однако определенные промоторы работают только в определенных организмах. Так, бактериальные промоторы не работают у растений и наоборот, растительные – в бактериях. Так как мы хотим, чтобы елка светилась ярко, то поставим ген под суперпромотор, который работает постоянно. Для растений им может являться промотор 35S из вируса мозаики цветной капусты.
К счастью на не нужно искать этот вирус и цветную капусту :) Можно купить уже готовую плазмиду, содержащую промотор и имеющую место для вставки гена. Например, такую как на рисунке.

Следующий шаг — мы выделяем плазмиду со вставкой из культуры бактерий и вырезаем оттуда ген. Вырезание производится с помощью ферментов-рестриктаз (просто к раствору плазмидной ДНК добавляем фермент и буфер для работы фермента). По бокам от встроенного нами гена в плазмиде содержатся участки ДНК (сайты рестрикции), которые ими узнаются и происходит разрезание.
Всегда нужно выбирать те рестриктазы, которые будут резать только в одном месте, не разрезая сам ген (определенная рестриктаза всегда узнает определенный сайт, который состоит обычно из 6 определенных нуклеотидов). Например, рестриктаза EcoR1 всегда разрежет ДНК если обнаружит в ней последовательность G'AATTC, причем резать будет и одну цепь и вторую.

Если рестриктаза режет не точно посередине последовательности узнавания, то по краям остаются так называемые “липкие концы”, где часть ДНК одноцепочечна. Такие концы имеют свойство “липнуть”- пристыковываться к другим липким концам с той же последовательностью одноцепочечных участков. Если последовательность будет иной, то стыковки не произойдет. Таким образом если мы вырежем ген двумя рестриктазами – одной для начала гена и другой для конца, то начало и конец его будут иметь разные концы, которые соединятся только с себе подобными. Это очень важно для контролирования ориентации гена, ведь работает он только если повернут определенным образом к служебным последовательностям.
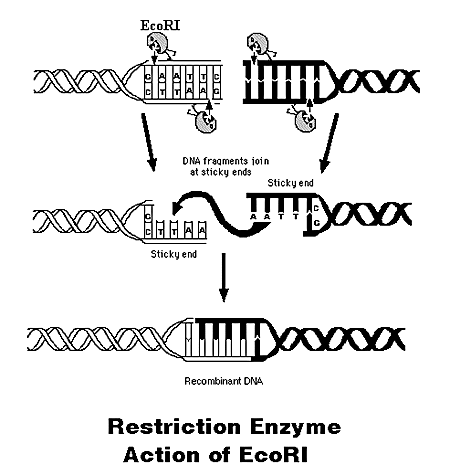
Некоторые рестриктазы могут порезать четко посередине и получим “тупые концы”. По тупым концам тоже можно сделать сшивку, но получится 50% вероятность пришить ген не той стороной которой нужно, а задом наперед.
После вырезания гена очищаем его от остатков плазмиды с помощью электрофореза.
Аналогичным образом разрезаем купленную плазмиду с промотором и смешиваем ее с вырезанным геном.
Добавляем лигазы и вуаля – имеем сшитую последовательность, где у нас имеется промотор 35S и ген bl1.
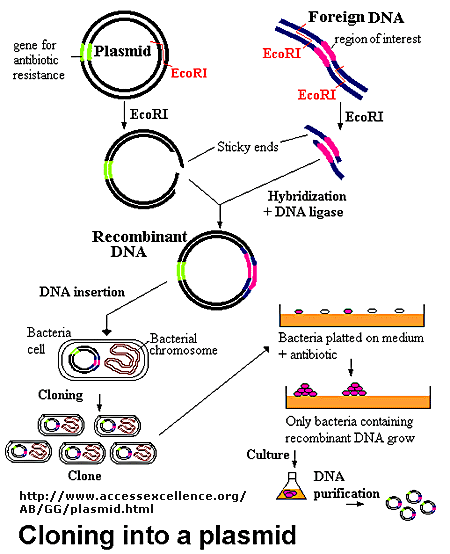
Снова трансформируем бактерии, уже этой полученной конструкцией. Так как мы ввели промотор, работающий у растений, то светиться такие бактерии не будут. Если бы мы ввели бактериальный промотор, то на этом шаге культура бактерий бы засветилась.
Плазмида с промотором, геном, маркёрами и другими служебными частями называется “плазмидой для экспрессии”. Ее уже можно использовать для получения трансгенных растений.
Это у нас второе сохранение. Мы уже знаем как заставить бактерии светиться и получили почти все необходимое, чтобы получить трансгенные растения.
Заметьте, процесс генноинженерной работы многоступенчатый и многозадачный. В реальной жизни одновременно происходит работа с 3-4 экспериментами находящимися на разных стадиях. Пока в одном растут бактерии, для другого мы проводим рестрикцию плазмиды, а для третьего выделяем ген. Происходит это из-за того, что никогда не бывает настолько идеально гладкого хода работ, как я описал, всегда возникают проблемы по разным причинам, их приходится обнаруживать, преодолевать. Даже на выявление ошибки на каждой стадии уходит минимум несколько часов.
И именно для преодоления проблем нужен весь объем знаний молекулярного биолога, а не для последовательного капанья из одной пробирки в другую, чем может заниматься и лаборант :)
Но о том, как же мы все-таки получим светящуюся синим елку, я расскажу в заключительной статье. Там же приведу список оборудования и реактивов, с ценами :)
UPD:
Часть 3, заключительная.
Краткое содержание предыдущей серии:
Ученые открыли ген синего свечения. Мы прочитали об этом гене и загорелись сделать светящуюся трансгенную елку. Нашли в специализированных ресурсах его название и последовательность, выбили командировку у шефа и скатались туда, где живет животное – бутявка, в которой содержится этот ген.
Путем различных ухищрений с применением специального оборудования мы получили чистые молекулы ДНК гена bl1, кодирующего белок синего свечения.
У нас есть ген. Чего же мы ждем, спросят читатели, давайте засунем этот ген в елку и она начнет светиться?
Не все так просто, и вот, почему.
Любой ген работает только когда с него считывается информация. В нашем случае это мРНК белка bl1. Более того, сама мРНК должна работать, но это отдельная история.
Второе – ген должен передаваться при делении клетки ее потомкам. Иначе все пойдет насмарку.
Третье – ведь ген это не булавка, его еще засунуть как-то нужно!
Если мы просто поместим в клетку ген, то ни информация с него не будет прочитана, ни передаваться он не будет (да, собственно, и с засовыванием его большие проблемы). Поэтому, мы должны навесить на него какую-нибудь служебную информацию, которая бы позволила ему работать и облечь в форму, которая позволит передаваться потомкам. А так же каким-то образом занести его в клетку.
Однако еще раньше мы постараемся сохранить имеющийся ген, чтобы в любой момент можно было его получить много и не ездить за бутявкой.
Первая трансформация.
Самая первая задача, которая стоит на каждом этапе – сохранить результаты предыдущих этапов. Актуальная задачи и в программировании, не правда ли? :)
Сейчас мы поместим наш ген в бактерию, так, чтобы в любой момент мы могли ее размножить и достать оттуда необходимое количество. Это будет наш первый трансгенный организм и процесс его создания называется трансформацией.
Почему мы просто не можем размножить ген с помощью ПЦР, как мы делали до этого? Дело в том, что вероятность ошибки в реакции ПЦР 1/10^3, а в бактерии 1/10^6, то есть копирование его происходит в тысячу раз точнее, а точность нам нужна абсолютная и чем больше, тем лучше.
Итак, помещаем ген в бактерию, как же это сделать? Для этого для начала подготовим контейнер — специальную кольцевую молекулу ДНК, называемую плазмидой. Эта плазмида может плавать в клетке бактерии независимо от ее генома, размножаться и передаваться потомкам, так как у нее есть необходимые для этого гены и сигнальные последовательности.
Так же в плазмиде есть гены маркёры. Это такие гены, которые помогут нам отобрать клетки с плазмидой, от клеток где ее нет. Маркёром, например, может быть ген окраски (бактерии с плазмидой будут окрашены) или устойчивости (бактерии с плазмидой не умрут на среде с антибиотиком).
Плазмиды можно купить в биотехнологической компании, их продают всем желающим. Прийдет она к вам в виде прозрачного раствора в небольшой пробирке (собственно, так же выглядит раствор любой другой ДНК). Для вставки гена в плазмиду ее нужно надрезать ферментом — рестриктазой (речь о ней пойдет далее), но часто они продаются уже надрезанными.
Допустим мы купили современную плазмиду, например pJET1,2 от Fermentas.

Вот она, красавица. В верхнем правом углу много мелких названий – это перечислены сайты рестрикции. Rep – это участок отвечающий за репликацию (размножение) плазмиды в клетке, а Amp – репортерный ген устойчивости к антибиотику – ампициллину.
К плазмиде поставляется набор реактивов, так называемый “кит”. Мы капаем по инструкции чуть чуть раствора нашего гена, плазмиды с реактивами из кита и фермента лигазы и получаем раствор, где молекулы плазмиды соединились с молекулами гена и получилась единая кольцевая молекула, содержащая ген bl1.
Такую плазмиду называют “плазмида со вставкой”.
Фермент лигаза сшивает пристыкованые друг к другу участки ДНК. Она сшивает все подряд и не может определить, правильно ли все пристыковано (например, может просто сшить плазмиду саму с собой, вовсе без нашего гена), поэтому наша задача делать так, чтобы стыковаться молекулы могли только определенным образом. Чуть дальше я расскажу об этом, когда пойдет речь о липких концах.
Плазмида pJet1,2 продается уже разрезанной посередине гена eco471R. Это ген кодирует клеточный яд – мощную рестриктазу, которая убъет клетку если лигаза сошьет плазмиду без вставленного гена bl1 и такая плазмида попадет в бактерию. Это очень удобно, так как нам не нужно беспокоиться, что вырастут бактерии, в которых вовсе нет вставки, что бывает с другими типами плазмид (этот тип назван плазмидой-самоубийцей или “selfkill plasmid”).
Изначально эта информация выходила за рамки статьи, но я подумал, что иначе будут вопросы, зачем этот ген :)
Далее берем специально подготовленную культуру бактерий кишечной палочки (Echerichia coli или E.coli) и по протоколу трансформации капаем в них раствор плазмиды со вставкой. Протоколы могут быть разные, вот пример. Бактерии очень легко поддаются трансформации, по сути ДНК просто в них проникает и все, никаких других ухищрений.
Обычно трансформацию делают вечером, наутро бактерии подрастают и мы уже имеем результаты.
На чашке Петри со средой для роста, имеется множество колоний. Каждая колония — потомки одной единственной трансформированной клетки. Мы выбираем некоторые из них, тестируем на содержание bl1 методом ПЦР (чтобы убедиться в наличии гена) и можем положить на хранение.
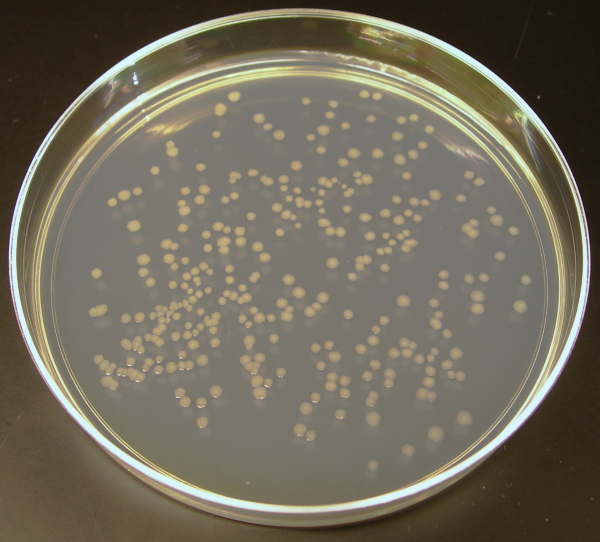
Бактерии растут очень быстро и теперь плазмиду с геном можно выделить из них в любой момент в нужном количестве
Итак, мы засейвились :) и параллельно получили культуру трансгенных бактерий. Будут они светиться или нет зависит от того, какую плазмиду для трансформации мы выбрали, есть ли в ней сигнальная последовательность для синтеза мРНК – промотор.
Отмечу, что вот такое сохранение промежуточных результатов всегда проводят в бактериях, независимо от того, с каким далее объектом происходит работа. Просто с ними очень удобно работать и хранить (быстро заморозив в жидком азоте).
Подготовка транскрибирующейся последовательности.
Чтобы последовательность гена работала в клетке, с нее должна прочитываться мРНК(а с нее — белок), то есть она должна транскрибироваться. Для того чтобы это произошло, перед геном обязательно должна стоять управляющая последовательность – промотор.
Промоторы есть у всех генов и они отвечают за то, в каких условиях должен синтезироваться ген, однако определенные промоторы работают только в определенных организмах. Так, бактериальные промоторы не работают у растений и наоборот, растительные – в бактериях. Так как мы хотим, чтобы елка светилась ярко, то поставим ген под суперпромотор, который работает постоянно. Для растений им может являться промотор 35S из вируса мозаики цветной капусты.
К счастью на не нужно искать этот вирус и цветную капусту :) Можно купить уже готовую плазмиду, содержащую промотор и имеющую место для вставки гена. Например, такую как на рисунке.

Следующий шаг — мы выделяем плазмиду со вставкой из культуры бактерий и вырезаем оттуда ген. Вырезание производится с помощью ферментов-рестриктаз (просто к раствору плазмидной ДНК добавляем фермент и буфер для работы фермента). По бокам от встроенного нами гена в плазмиде содержатся участки ДНК (сайты рестрикции), которые ими узнаются и происходит разрезание.
Всегда нужно выбирать те рестриктазы, которые будут резать только в одном месте, не разрезая сам ген (определенная рестриктаза всегда узнает определенный сайт, который состоит обычно из 6 определенных нуклеотидов). Например, рестриктаза EcoR1 всегда разрежет ДНК если обнаружит в ней последовательность G'AATTC, причем резать будет и одну цепь и вторую.

Если рестриктаза режет не точно посередине последовательности узнавания, то по краям остаются так называемые “липкие концы”, где часть ДНК одноцепочечна. Такие концы имеют свойство “липнуть”- пристыковываться к другим липким концам с той же последовательностью одноцепочечных участков. Если последовательность будет иной, то стыковки не произойдет. Таким образом если мы вырежем ген двумя рестриктазами – одной для начала гена и другой для конца, то начало и конец его будут иметь разные концы, которые соединятся только с себе подобными. Это очень важно для контролирования ориентации гена, ведь работает он только если повернут определенным образом к служебным последовательностям.

Некоторые рестриктазы могут порезать четко посередине и получим “тупые концы”. По тупым концам тоже можно сделать сшивку, но получится 50% вероятность пришить ген не той стороной которой нужно, а задом наперед.
После вырезания гена очищаем его от остатков плазмиды с помощью электрофореза.
Аналогичным образом разрезаем купленную плазмиду с промотором и смешиваем ее с вырезанным геном.
Добавляем лигазы и вуаля – имеем сшитую последовательность, где у нас имеется промотор 35S и ген bl1.

Снова трансформируем бактерии, уже этой полученной конструкцией. Так как мы ввели промотор, работающий у растений, то светиться такие бактерии не будут. Если бы мы ввели бактериальный промотор, то на этом шаге культура бактерий бы засветилась.
Плазмида с промотором, геном, маркёрами и другими служебными частями называется “плазмидой для экспрессии”. Ее уже можно использовать для получения трансгенных растений.
Это у нас второе сохранение. Мы уже знаем как заставить бактерии светиться и получили почти все необходимое, чтобы получить трансгенные растения.
Заметьте, процесс генноинженерной работы многоступенчатый и многозадачный. В реальной жизни одновременно происходит работа с 3-4 экспериментами находящимися на разных стадиях. Пока в одном растут бактерии, для другого мы проводим рестрикцию плазмиды, а для третьего выделяем ген. Происходит это из-за того, что никогда не бывает настолько идеально гладкого хода работ, как я описал, всегда возникают проблемы по разным причинам, их приходится обнаруживать, преодолевать. Даже на выявление ошибки на каждой стадии уходит минимум несколько часов.
И именно для преодоления проблем нужен весь объем знаний молекулярного биолога, а не для последовательного капанья из одной пробирки в другую, чем может заниматься и лаборант :)
Но о том, как же мы все-таки получим светящуюся синим елку, я расскажу в заключительной статье. Там же приведу список оборудования и реактивов, с ценами :)
UPD:
Часть 3, заключительная.